RESUMEN
El descubrimiento del ácido gamma-hidroxibutirato (GHB) hace más de 40 años condujo a su uso inmediato como agente anestésico general. Investigaciones posteriores demostraron que el GHB es un compuesto endógeno en el cerebro de los mamíferos y la investigación actual sugiere que el GHB es probablemente un neurotransmisor. En los Estados Unidos, los informes de efectos anabólicos llevaron a su uso indebido entre culturistas durante la década de 1980, mientras que las propiedades tóxicas de la droga llevaron a su popularización como sustancia de abuso durante la década de 1990, sobretodo en el movimiento de las “raves”. El GHB se asoció con informes de agresión sexual facilitada por drogas y casos de dependencia física y abstinencia. Los esfuerzos para prohibir el GHB provocaron un mayor uso de análogos y profármacos del GHB.
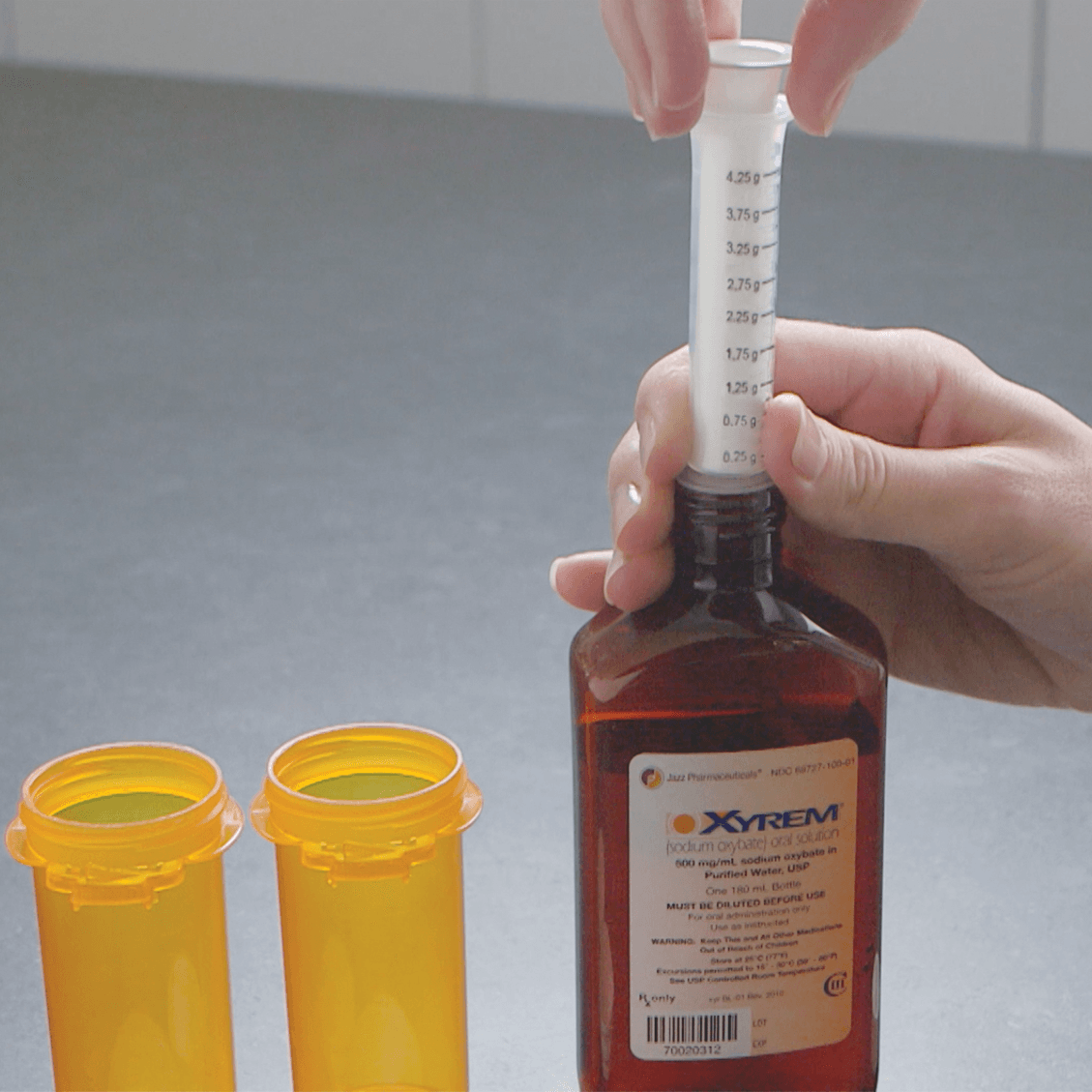
En este contexto, el GHB se estaba desarrollando para el tratamiento de la narcolepsia, lo que llevó a la aprobación de la solución oral Xyrem® (oxibato de sodio) en 2002, para el tratamiento de la cataplejía en pacientes con narcolepsia. Un programa de gestión de riesgos permite la manipulación y distribución seguras del producto aprobado, minimiza el riesgo de desvío, brinda educación a profesionales y pacientes sobre los riesgos y beneficios del oxibato de sodio e incluye registros de médicos y pacientes. La vigilancia posterior a la comercialización indica que el oxibato de sodio tiene un perfil de seguridad aceptable y presenta un riesgo mínimo de desarrollo de dependencia física.
INTRODUCCIÓN
La solución oral de Xyrem® (oxibato de sodio), una preparación farmacéutica de gamma-hidroxibutirato (GHB), se desarrolló para el tratamiento de la narcolepsia en medio de la controversia en torno al creciente abuso de GHB y los informes de su uso para facilitar la agresión sexual. La narcolepsia es un trastorno del sueño de por vida descrito clásicamente como una tétrada de síntomas que consiste en somnolencia diurna excesiva, cataplejía, parálisis del sueño y alucinaciones hipnagógicas.
La somnolencia diurna excesiva resulta de la incapacidad de lograr un sueño reparador, mientras que se cree que los síntomas restantes representan la expresión inapropiada del sueño, de movimientos oculares rápidos (REM) durante la vigilia. Además, los pacientes con narcolepsia pueden sufrir sueño nocturno fragmentado, conductas automáticas, problemas de concentración mental y memoria, y alteraciones visuales y sensoriales. Este documento analiza el desarrollo clínico del oxibato de sodio y describe los pasos que se tomaron para abordar los problemas de seguridad y cómo se superaron los desafíos regulatorios. También se presentan detalles del programa integral de gestión de riesgos que se estableció y los resultados de más de 2 años de vigilancia posterior a la comercialización. Durante más de 40 años desde su descubrimiento, el gamma hidroxibutirato se ha empleado adecuadamente en la medicina clínica para el tratamiento de un trastorno raro y está preparado para una mayor investigación y desarrollo clínico, lo que puede resultar en un tratamiento beneficioso de las necesidades no satisfechas de otras poblaciones de pacientes.
NEUROFISIOLOGÍA
El GHB fue descubierto en 1960 por Henri Laborit mientras buscaba análogos terapéuticamente útiles del ácido gamma aminobutírico (GABA), un neurotransmisor inhibidor. Más tarde se descubrió que era una sustancia natural en el cerebro y en muchos tejidos periféricos. La síntesis in vivo en el cerebro ocurre principalmente por el metabolismo de GABA a semialdehído succínico y reducción a GHB. Por el contrario, el metabolismo del GHB implica la conversión oxidativa en semialdehído succínico y luego en ácido succínico, que entra en el ciclo de Krebs. Así, el GHB se metaboliza a dióxido de carbono y agua, sin metabolitos activos. Las rutas menores del metabolismo del GHB incluyen la conversión a GABA por oxidación (Figura 1) .
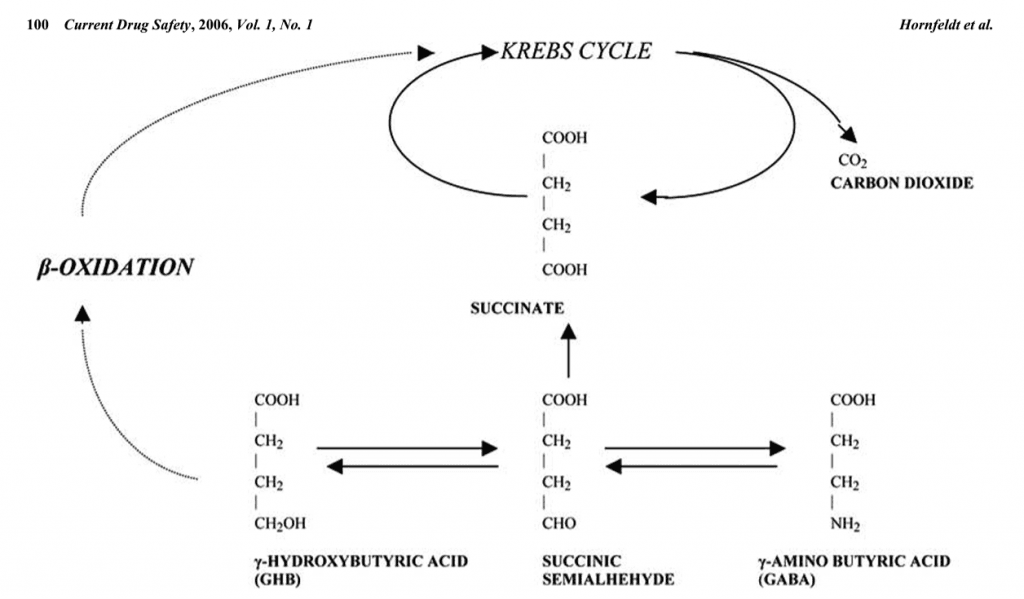
La necesidad de una mejor comprensión del papel del GHB como compuesto endógeno se ha hecho aún más evidente por la descripción de un aparente error innato del metabolismo del GHB debido a una deficiencia en la succínico semialdehído deshidrogenasa (SSADH). Esta deficiencia provoca una acumulación endógena de GHB, GABA y productos de su oxidación, lo que lleva a problemas motores que incluyen ataxia, hiporreflexia, convulsiones, retraso mental, hipercinesia, psicosis y muchas otras manifestaciones neurológicas. Aunque el GHB normalmente no es detectable en individuos sanos, se ha demostrado que el GHB acumulado en pacientes con este trastorno alcanza concentraciones plasmáticas de hasta 100 g/mL en individuos afectados.
Una cantidad sustancial de evidencias respaldan el papel del GHB como neurotransmisor en el sistema nervioso central (SNC)]. Específicamente, después de la síntesis neuronal, el GHB se ubica dentro de vesículas de almacenamiento axonal discretas, donde posteriormente se libera de una manera dependiente del calcio y la recaptación se produce a través de un sistema de transporte de membrana de alta afinidad dependiente del sodio. El GHB se une a sitios de unión de alta y baja afinidad ubicados en el tejido neural, que tienen una alta especificidad por el GHB .
Aunque la función específica de lo que ocurren naturalmente con el GHB, más allá de la posible neuromodulación se desconoce en este momento, la administración de GHB exógeno da como resultado varias acciones dentro del sistema nervioso central, incluida una dosis-aumento dependiente de la concentración de dopamina, aumento del recambio de serotonina y liberación de la hormona del crecimiento.
Además del SNC, muchos órganos periféricos contienen GHB. Las concentraciones de GHB en el corazón, los riñones, el músculo esquelético y la grasa son considerablemente más altas que en el cerebro, lo que sugiere que puede participar en procesos metabólicos en estos tejidos. Por ejemplo, existe evidencia de que el GHB puede reducir el consumo de sustratos energéticos en el cerebro y los tejidos periféricos y que puede proteger a estos tejidos de los efectos dañinos de la anoxia o la demanda metabólica excesiva. A la luz de estos hallazgos, es interesante resaltar, que se ha encontrado que las concentraciones endógenas de GHB son significativamente elevadas después de la muerte. Las implicaciones clínicas de estos hallazgos quedan por dilucidar.
USO CLÍNICO TEMPRANO
Poco después de su descubrimiento, Laborit describió los méritos del GHB como agente anestésico y también sugirió posibles efectos beneficiosos en obstetricia, psiquiatría, síndromes de abstinencia de alcohol y opiáceos e incluso en el metabolismo de los lípidos.
Aunque el GHB se ha empleado clínicamente en Europa en el campo de la anestesia, no tiene propiedades analgésicas y debe usarse en combinación con un analgésico opiáceo u otro agente anestésico. Durante la inducción y la salida de la anestesia con GHB, pueden ocurrir movimientos clónicos aleatorios (mioclono). Por lo tanto, el GHB nunca obtuvo una aceptación generalizada como agente anestésico general.
Curiosamente, se encontró que la administración de GHB a la hora de acostarse no cambió significativamente el ciclo de sueño normal medido por EEG y por esta razón, los primeros investigadores plantearon la hipótesis de que el GHB puede ser beneficioso para el tratamiento de los trastornos del sueño nocturno. La marcada alteración del sueño nocturno en pacientes con narcolepsia, llevó a Broughton y Mamelak a usar GHB en un intento de normalizar el sueño en estos pacientes con la esperanza de que esto ayudaría a controlar los síntomas diurnos. Este tratamiento produjo mejoras inmediatas en la calidad subjetiva del sueño nocturno y produjo una mejora gradual en los síntomas diurnos de la narcolepsia. De hecho,a los pacientes de estos primeros estudios les resultó más fácil permanecer despiertos durante el día y los ataques de cataplejía prácticamente desaparecieron.
Estos y posteriores ensayos demostraron que la administración nocturna de GHB aumentó el tiempo total de sueño nocturno, disminuyó los despertares nocturnos y aumentó la duración total de las etapas 3 y 4 del sueño. Estas mejoras en el sueño nocturno también se asociaron con mejoras en los ataques de sueño diurno, cataplejía, parálisis del sueño y alucinaciones hipnagógicas. Los prometedores resultados de estos ensayos conducen al desarrollo clínico formal del oxibato de sodio, que se analiza a continuación.
ABUSO DE GHB
Durante la década de 1980, el GHB se había comercializado en los EE. UU. como suplemento dietético no regulado en tiendas naturistas, gimnasios y centros de acondicionamiento físico. Los beneficios anabólicos, supuestamente se produjeron al estimular la liberación de la hormona del crecimiento y fue utilizado por los culturistas y para el entrenamiento de fuerza. Además, se promocionó como un tratamiento “natural” para el insomnio y para inducir la pérdida de peso. Tras los informes de sobredosis fatales entre varios culturistas en California y Florida, la FDA prohibió todas las ventas de GHB en 1990.
Desafortunadamente, estos pasos hicieron poco para frenar el abuso de GHB. Las restricciones impuestas a la venta de GHB por la FDA y las regulaciones estatales más estrictas llevaron a un aumento del GHB sintetizado ilegalmente y al uso de los llamados análogos de GHB, como gamma-butirolactona (GBL), 1,4-butanodiol (1,4 – BD), que sirven como profármacos porque se metabolizan a GHB in vivo. Los productos que contienen estos compuestos industriales rápidamente estuvieron disponibles a través de varias fuentes, incluida Internet. GBL también se vendió sin receta en forma de kit con hidróxido de sodio e instrucciones para la síntesis casera de GHB. Como estos análogos se convierten en GHB después de la ingestión, GBL y 1,4-BD producen manifestaciones clínicas similares a las del GHB, aunque pueden variar en potencia y propiedades toxicocinéticas.
A mediados de la década de 1990, las versiones caseras y otras versiones ilícitas del GHB habían adquirido notoriedad como «drogas de club» y se usaban ampliamente en las «raves» o fiestas de baile que duraban toda la noche.
Los usuarios recreativos de la droga afirman experimentar una euforia similar al alcohol, desinhibición y excitación sexual sin efectos desagradables de resaca. También en ese momento, varios usuarios de GHB estaban experimentando una sobredosis aguda, a menudo como consecuencia de la combinación de GHB con otras drogas de abuso y etanol.
El GHB también estuvo implicado en una serie de casos de agresión sexual y, al igual que el flunitrazepam (Rohipnol®, Hoffman LaRoche, Inc.), estaba siendo etiquetado como una droga de «violación en citas» en los EE. UU. Como muchos depresores del SNC, el GHB causa amnesia anterógrada, especialmente cuando se combina con etanol, lo que a menudo impide que la víctima recuerde ningún detalle del evento.
Al final de la década, se reconocieron las graves consecuencias del abuso crónico, incluida la dependencia y la abstinencia. Se han informado abusos durante largos períodos de tiempo, que van desde meses hasta años. Algunos abusadores supuestamente aumentaron su ingesta diaria de GHB a aproximadamente 150 g por día. Curiosamente, los estudios en animales sugieren que el GHB tiene un bajo potencial de abuso.
El aumento de la dosis, asociado con una mayor frecuencia de dosificación (con dosificación informada cada 30 minutos a tres horas durante todo el día), forma la base del síndrome de abstinencia. Se ha notificado un síndrome distinto tras el cese repentino de formas ilícitas de GHB, que puede persistir durante 5 a 15 días. Los síntomas han incluido náuseas, vómitos, ansiedad, confusión, temblor, insomnio, agitación, psicosis, alucinaciones auditivas y visuales, taquicardia e hipertensión. Para algunas de estas personas, los síntomas de abstinencia pueden ser graves y requerir dosis extremadamente altas de benzodiazepinas. El pentobarbital se ha utilizado con éxito y el propofol también se ha sugerido como una alternativa cuando las benzodiazepinas son insuficientes.
OBSTÁCULOS LEGALES PARA EL DESARROLLO DE SOLUCIÓN ORAL DE OXIBATO DE SODIO
El desarrollo clínico formal del oxibato de sodio para el tratamiento de la narcolepsia comenzó en 1994. La Organización Nacional de Trastornos Raros (NORD) y la División de Desarrollo de Productos Huérfanos de la Administración de Alimentos y Medicamentos (FDA) se acercaron a Orphan Medical, cada uno de los cuales sugirió el desarrollo de GHB narcolepsia Esta sugerencia se basó en los prometedores resultados obtenidos por varios investigadores independientes, como se discutió anteriormente, quienes informaron sobre la eficacia del oxibato de sodio (GHB) como tratamiento para la narcolepsia. En estos primeros ensayos clínicos, la administración nocturna de oxibato de sodio mejoró en gran medida la calidad del sueño nocturno en pacientes con narcolepsia con una reducción asociada de los ataques de sueño diurno, cataplejía y otros síntomas de narcolepsia.
Sin embargo, a fines de la década de 1990, había una conciencia bien establecida de la escala y las consecuencias de la epidemia de abuso de GHB y análogos relacionados. El creciente número de casos de abuso, sobredosis mortales y agresión sexual facilitada por drogas llevó a la Agencia de Control de Drogas (DEA) a comenzar el proceso formal de elaboración de normas para controlar el GHB. Esta acción amenazó con obstaculizar en gran medida el desarrollo futuro de GHB para fines medicinales legítimos.
Un tema principal fue la aplicación de una Lista de medicamentos que aplicaría las sanciones penales más severas posibles por el uso ilícito y la distribución ilegal de GHB y sustancias químicas relacionadas, pero permitiría el acceso al oxibato de sodio a los pacientes que lo necesiten. Por lo tanto, los miembros del Congreso fueron desafiados a idear una solución legislativa aceptable, que abordara las necesidades urgentes de las fuerzas del orden público y los pacientes con enfermedades raras. La legislación resultante fue la Ley de Prohibición de Drogas de Violación de Hillory J. Farias y Samantha Reid de 2000 (Ley Pública [PL] 106-172). Esta ley estipuló una nueva programación bifurcada y ordenó al Fiscal General de los EE. UU. que enmendara la Ley de Sustancias Controladas al incluir al GHB como un agente de la Lista I y crear una excepción para colocar las formulaciones de GHB aprobadas por la FDA en la Lista III.
Además, GBL fue designado como un químico de la Lista I. Una disposición adicional a esta ley promovió la evaluación continua del oxibato de sodio como medicamento huérfano al permitir condiciones de almacenamiento de la Lista III para productos farmacéuticos en investigación que contienen GHB. La nueva ley también dejó en claro que el uso de cualquier forma de GHB para facilitar la agresión sexual era un delito federal y que la posesión o distribución ilícita de cualquier forma de GHB estaría sujeta a las sanciones penales del Anexo I.
Aunque cada estado tiene la opción de imponer una programación más restrictiva que las pautas federales, el estado innovador de la Lista I/III promovido por el Congreso ha sido adoptado por 44 estados en los EE. UU. y la programación específica del estado está vigente en otros 5 estados. A partir de junio de 2005, la legalización del uso de recetas aún está pendiente en Oklahoma.
EL DESARROLLO CLÍNICO DEL SODIO SOLUCIÓN ORAL DE OXIBATO
Orphan Medical estableció la seguridad y la eficacia del oxibato de sodio para el tratamiento de la cataplejía asociada con la narcolepsia en dos estudios multicéntricos, aleatorizados, doble ciego, controlados con placebo y de grupos paralelos (ensayos A, B). Se proporcionaron datos de seguridad adicionales mediante un ensayo abierto a largo plazo, el Ensayo C, una extensión abierta de 12 meses del Ensayo A, en el que las dosis de oxibato de sodio se ajustaron a la respuesta clínica óptima para cada paciente.
Los detalles de estos ensayos patrocinados por Orphan Medical se proporcionan en la Tabla 1. Los resultados de estos ensayos, además de los resultados de dos ensayos pequeños realizados por investigadores, formó la base para la aprobación del oxibato de sodio para el tratamiento de la cataplejía en pacientes con narcolepsia en los EE. UU.
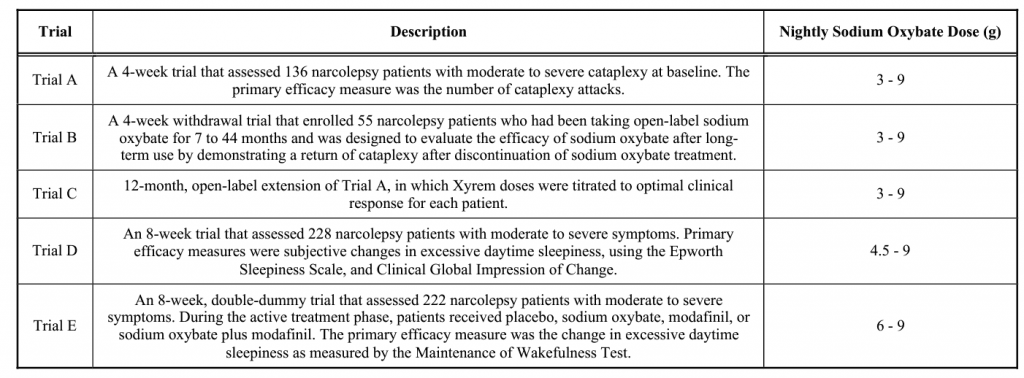
Los resultados alentadores de estos ensayos sobre los síntomas de la somnolencia diurna y los resultados de un estudio piloto sobre el efecto del oxibato de sodio en la arquitectura del sueño y el estado de alerta diurno conducen a dos ensayos multicéntricos (ensayos D y E), que evalúan los efectos del oxibato de sodio sobre la arquitectura del sueño y el funcionamiento diurno (Tabla 1). Los resultados de estos ensayos sobre el tratamiento de la somnolencia diurna excesiva, mostraron resultados prometedores y se incluyeron en una nueva solicitud de fármaco complementaria presentada a la FDA en enero de 2005 en busca de indicaciones más amplias para el tratamiento de la narcolepsia.
Los datos de estos ensayos clínicos indican que la administración nocturna de oxibato de sodio para el tratamiento de la narcolepsia está asociada con mejoras significativas en el sueño nocturno, incluidos aumentos relacionados con la dosis en el sueño de ondas lentas y disminuciones en el sueño nocturno. despertares. Estas mejoras coincidieron con mejoras en cataplexia y medidas subjetivas y objetivas de somnolencia diurna.
Datos de seguridad
El siguiente resumen de seguridad se basa en los datos combinados de los tres grandes estudios de grupos paralelos: Ensayo A, Ensayo D y Ensayo E. Tenga en cuenta que los datos de los pacientes del Ensayo B no se han incluido en este resumen. Todos los pacientes en ese ensayo habían sido reclutados de otros estudios en los que fueron tratados con oxibato de sodio durante seis meses o más, y luego fueron aleatorizados en forma doble ciego para continuar con el tratamiento con oxibato de sodio o placebo. El retorno de la cataplejía en pacientes tratados con placebo se utilizó como prueba de la eficacia a largo plazo del fármaco; sin embargo, se consideró poco probable que los eventos emergentes del tratamiento, en este paradigma de abstinencia, fueran los mismos que los de los pacientes recién iniciados en el tratamiento con oxibato de sodio.
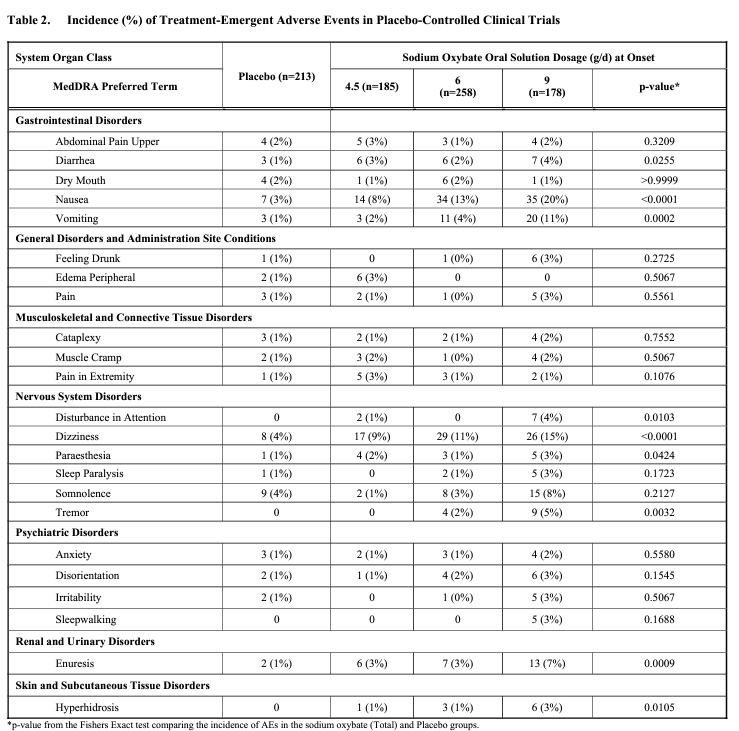
La Tabla 2 enumera la incidencia de eventos adversos emergentes del tratamiento, para los cuales hubo una incidencia de > 2 % en cualquier grupo de dosificación con más de 100 pacientes, y la incidencia en al menos un grupo de dosificación del fármaco fue mayor que la del placebo. El número de pacientes en cada grupo de dosificación representa el número total de pacientes tratados en cada dosis.
Los eventos adversos más comunes fueron náuseas, mareos, vómitos, somnolencia y enuresis. Ciertos eventos adversos fueron significativamente más comunes durante el tratamiento con oxibato de sodio que con el placebo: diarrea, náuseas, vómitos, alteración de la atención, mareos, parestesia, temblor, enuresis e hiperhidrosis. Las interrupciones del tratamiento, debido a eventos adversos, fueron más comunes con la dosis más alta de oxibato de sodio. Se observó una relación dosis-respuesta para náuseas, vómitos, parestesia, desorientación, irritabilidad, alteración de la atención, ebriedad, sonambulismo y enuresis, siendo la incidencia de estos eventos notablemente superior a 9 g/d. El mareo fue más común con 3 y 9 g/d.
Las posibles interacciones farmacocinéticas de los medicamentos, se analizaron en estudios de Fase I con otros medicamentos comúnmente recetados en pacientes con narcolepsia, específicamente, zolpidem, protriptilina y modafinilo. Estos fueron estudios de dosis única en los que los voluntarios recibieron oxibato de sodio, solo y junto con uno de los medicamentos mencionados anteriormente como dosis única, después de un período de lavado de una semana. No se demostraron interacciones farmacocinéticas. También se evaluó el potencial de interacciones farmacológicas por inhibición de las isoenzimas del citocromo P450 (CYP) microsomal hepático humano. El oxibato de sodio no afectó la actividad de las isoenzimas CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP2E1 o CYP3A humanas]. Por lo tanto, no se prevén interacciones metabólicas con la gran cantidad de fármacos metabolizados a través de estas vías. Los fármacos antiepilépticos ácido valproico, etosuximida y los barbitúricos inhiben la conversión de GHB a succínico semialdehído mediante el bloqueo de la GHB deshidrogenasa dependiente de NADP, lo que puede conducir a la potenciación de los efectos del GHB (Maitre 1997).
Programa de gestión de riesgos
Coincidiendo con el desarrollo clínico del oxibato de sodio, se dio la creación e implementación del concepto de gestión de riesgos en los EE. UU. En última instancia, el objetivo de la gestión de riesgos es asegurarse de que los productos farmacéuticos, se desarrollan, prueban, fabrican, etiquetan, prescriben, dispensan y utilizan, de una manera que maximiza beneficio para los pacientes y minimiza el riesgo de desviación y mal uso. La gestión de riesgos va más allá de lo habitual en reglamentos sobre etiquetado, promoción y publicidad, para involucrar actividades como la educación obligatoria para los proveedores de atención médica y pacientes; distribución restringida de productos; post-comercialización; un proceso simplificado para retirar el medicamento del mercado en caso de la retirada del producto; prescribir restricciones a poblaciones específicas de pacientes; uso de registros de médicos y pacientes, y/o establecimiento de un método completo para supervisar la prescripción, dispensación y uso del medicamento.
Debido a la creciente aprensión por el riesgo de posible desvío de medicamentos tras la aprobación del sodio oxibato y preocupaciones sobre el uso seguro, Orphan Medical colaboró con la FDA, expertos en desvío de medicamentos, prevención del abuso y médicos para crear un programa de gestión de riesgos. Los objetivos de este programa son: garantizar la distribución responsable de oxibato de sodio a pacientes con narcolepsia y educar a los médicos y pacientes sobre el uso seguro y responsable del oxibato de sodio. Los elementos del programa de gestión de riesgos incluyen:
- Una sola farmacia centralizada alojada en un lugar seguro.
- Registros de médicos y pacientes.
- Materiales educativos de Xyrem Success Program® para pacientes y médicos, y instalaciones.
- Un programa de evaluación post-comercialización (PMEP) para la vigilancia de eventos adversos.
A diferencia de las farmacias tradicionales, la farmacia central mantiene registros integrales de pacientes y médicos y verifica la elegibilidad de todos los médicos que lo recetan. Los farmacéuticos están capacitados para estar alertas ante problemas de cumplimiento, como dosis de medicamentos que aumentan rápidamente, intervalos de recarga cortos y preguntas o comportamientos sospechosos por parte de médicos o pacientes.
También brindan asesoramiento continuo para monitorear la seguridad del paciente, el cumplimiento y brindan apoyo educativo y clínico para pacientes y prescriptores.
A cada médico que desea recetar oxibato de sodio se le envía el Xyrem Success Program® con materiales educativos para médicos. Estos materiales brindan pautas de tratamiento para que los médicos las consideren al recetar oxibato de sodio.
También se alienta a los médicos a asesorar a sus pacientes sobre la dosificación y administración adecuadas de oxibato de sodio, a evaluar a los pacientes cada tres meses y volver a escribir las recetas de oxibato de sodio en intervalos de tres meses.
Después de que la farmacia recibe una nueva receta, se le envía al paciente el material educativo del Xyrem Success Program para pacientes, si su médico aún no se lo ha proporcionado. El programa contiene información que les enseña aspectos importantes sobre la eficacia y la seguridad del producto, les advierte sobre los peligros de combinar el oxibato de sodio con alcohol u otros medicamentos sedantes, y los alienta a no conducir un automóvil, ni realizar tareas peligrosas, hasta 6 horas después. la última dosis de oxibato de sodio. Antes de enviar el medicamento, un farmacéutico se pone en contacto con el paciente para confirmar que comprende la información del Xyrem Success Program para pacientes y para abordar cualquier pregunta adicional o preocupaciones.
El oxibato de sodio se envía al paciente mediante un servicio de envío nocturno. El paciente o su designado debe estar disponible para firmar la receta o será devuelta a la farmacia. El personal de farmacia también se pone en contacto con el paciente para asegurarse de que ha recibido su receta.
La farmacia central registra todos los informes de robo, pérdida o posible desvío de oxibato de sodio en un Informe de riesgo de desvío que se resume y se informa a la FDA trimestralmente. Desde el lanzamiento comercial del oxibato de sodio en septiembre de 2002 hasta el 31 de marzo de 2005, 8.391 pacientes registrados han recibido oxibato de sodio. La farmacia central completó un total de 20 informes de riesgo de desvío durante este período, que consisten en informes de pérdida, robo, problemas de entrega de mensajería e incumplimiento del paciente.
La vigilancia post-comerzcialización
Como condición para la aprobación de la FDA, en consideración de la base de datos de seguridad relativamente pequeña generada en los primeros ensayos clínicos, se implementó un programa de evaluación posterior a la comercialización (PMEP) para proporcionar a la FDA información sobre los primeros 6 meses de terapia con oxibato de sodio en 1000 pacientes. Cada médico prescriptor debe solicitar la aparición de eventos adversos de especial interés, en sus pacientes, en las visitas a la clínica a los 3 y 6 meses. De especial interés son los informes de eventos potencialmente graves, como vómitos, incontinencia urinaria (enuresis), sonambulismo, confusión o convulsiones. Además, los médicos pueden usar estos formularios para registrar información sobre sospechas de abuso o mal uso del oxibato de sodio por parte del paciente. Toda la información obtenida se registra en formularios de evaluación, incluidos con los materiales del Xyrem Success Program para médicos, que luego se envían por fax o por correo a una agencia independiente de seguridad de medicamentos para la gestión de datos.
Hasta el 30 de septiembre de 2004 se habían recibido un total de 695 informes de PMEP, que representan 460 pacientes únicos. No se informaron eventos adversos en 467 de estos informes (67% de todos los informes recibidos). El número de informes de «ningún evento adverso» después de menos de 3 meses, 3-6 meses, 6-9 meses y más de 9 meses de terapia con oxibato de sodio fue 184, 136, 79 y 54, respectivamente. La incidencia de muchos eventos adversos ocurrió con una frecuencia mucho menor que la citada actualmente en la etiqueta del producto. Por ejemplo, la incidencia de sonambulismo y convulsiones fue mucho menor que la informada anteriormente.
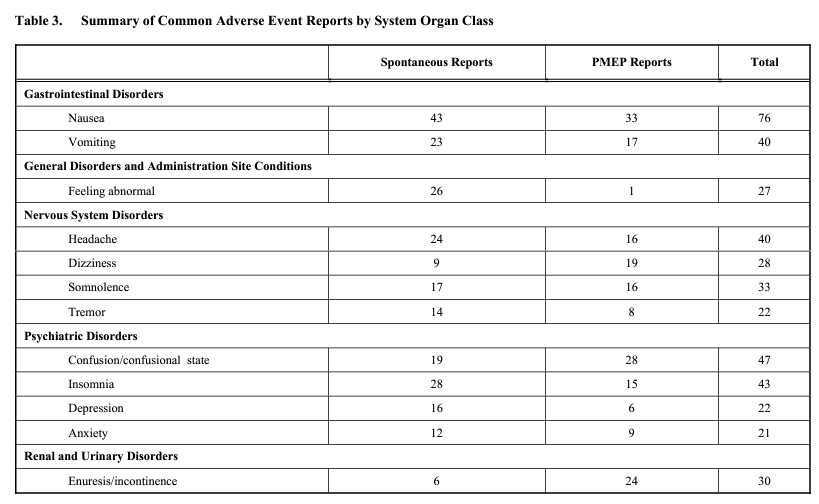
La Tabla 3 resume los eventos adversos informados con mayor frecuencia (20 o más), tanto de los informes espontáneos como de los informes derivados del PMEP. Estos eventos adversos informados comúnmente son consistentes con los identificados en estudios clínicos. A pesar de la exposición bastante extensa del producto, no se identificaron nuevos problemas de seguridad al analizar la base de datos de seguridad posterior a la comercialización del oxibato de sodio.
El impacto de la programación bifurcada de GHB se puede medir indirectamente por las tendencias en las visitas al departamento de emergencias, relacionadas con el abuso de drogas que involucran GHB. La Red de Alerta de Abuso de Drogas (DAWN) es un sistema de vigilancia de Salud Pública que monitorea las visitas al departamento de emergencias de los hospitales, relacionadas con las drogas y las muertes relacionadas, con el fin de identificar las tendencias del abuso de drogas en los EE. UU. Actualmente, estos datos se limitan a informes obtenidos de 260 hospitales, en 21 áreas metropolitanas; sin embargo, estos datos sugieren que las visitas al departamento de emergencias, relacionadas con GHB alcanzaron su punto máximo en 2000, año en que se promulgó la Ley de Prohibición de Drogas de Violación de Hillory J. Farias y Samantha Reid de 2000. Las visitas al servicio de urgencias se redujeron en un tercio en 2001 y mostraron un ligero descenso al año siguiente. A partir de 2003, se iniciaron importantes funciones nuevas de DAWN, incluido un cambio en el método por el cual se recopilan los datos y se amplió el alcance para incluir visitas al servicio de urgencias relacionadas con el uso de medicamentos con fines terapéuticos legítimos. Como resultado, ya no es posible la comparación directa de los datos de 2003 con los de años anteriores; sin embargo, se registró un total de 990 visitas por GHB en el tercer y cuarto trimestre de 2003 en comparación con aproximadamente 47 000 visitas por heroína y 120 000 visitas por cocaína.
Los informes a los centros de intoxicación, de exposiciones a GHB o sus análogos, han mostrado una disminución similar desde la promulgación de la Ley de Prohibición de Drogas de Violación de Hillory J. Farias y Samantha Reid de 2000. El número de exposiciones a GHB o sus análogos ha disminuido de 1,916 en 2001 (el primer año en que se recopilaron datos sobre GHB) a 800 exposiciones en 2003, una disminución del 58 %. Con base en estos hallazgos, el lanzamiento comercial del oxibato de sodio en 2002 no parece haber contribuido de manera sustancial al abuso de GHB.
CONCLUSIÓN
Coincidente con el desarrollo clínico del sodio oxibato para el tratamiento de la narcolepsia estaban creciendo preocupaciones sobre el uso indebido, abuso potencial de GHB, temores de desvío y disponibilidad comercial y preocupaciones de dependencia. Siguiendo la legislación federal, que creó una Lista bifurcada única I/III para GHB/sodio ilícito oxibato, los informes de aparente abuso de GHB ilícito parecen estar disminuyendo constantemente. La implementación de un programa de gestión de riesgos, ha puesto el oxibato de sodio a disposición de miles de pacientes mientras que existen pocos informes de sospecha de que se haya producido desvío. No hay casos de dependencia física y el perfil de seguridad general en uso clínico parece ser superior a lo que era observado originalmente durante los ensayos clínicos.
Wedin, G., Hornfeldt, C., & Ylitalo, L. (2008).The Clinical Development of Gamma;-Hydroxybutyrate (GHB). In Current Drug Safety (Vol. 1, Issue 1, pp. 99–106).